Függetlenül attól, hogy egy gyógyszert az orvos írt fel, vény nélkül vásárolták vagy illegálisan szerezték be, többnyire természetesnek vesszük a hatásmechanizmusukat, és bízunk abban, hogy megteszik, amit kellene.
De hogyan kapcsolja ki az ibuprofen tabletta a fejfájást? És mit tesz az antidepresszáns, hogy segítsen egyensúlyban tartani az agyi kémiát?
Valami oly hihetetlennek tűnő dolog esetében a gyógyszermechanika csodálatosan egyszerű. Ez leginkább a receptorokról és az őket aktiváló molekulákról szól.
receptorok
A receptorok nagy fehérjemolekulák, amelyek a sejtfalba vagy membránba vannak ágyazva. Kémiai információkat kapnak (tehát „receptorok”) más molekuláktól - például gyógyszerektől, hormonoktól vagy neurotranszmitterektől - a sejten kívül.
Ezek a külső molekulák a sejtben található receptorokhoz kötődnek, aktiválják a receptort, és biokémiai vagy elektromos jelet generálnak a sejtben. Ez a jel ekkor bizonyos dolgokra készteti a sejtet, például fájdalmat éreztet bennünket.
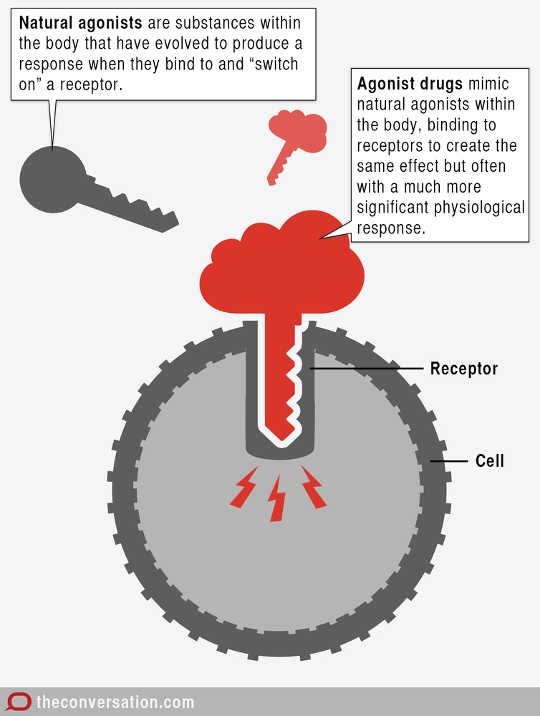
Agonista gyógyszerek
Azokat a molekulákat, amelyek specifikus receptorokhoz kötődnek, és a sejtben egy folyamat aktivizálódását okozzák, agonistáknak nevezzük. Az agonista valami, ami specifikus élettani választ okoz a sejtben. Lehetnek természetesek vagy mesterségesek.
Például az endorfinok az opioid receptorok természetes agonistái. De a morfium - vagy heroin, amely a szervezetben morfinná alakul - a fő opioidreceptor mesterséges agonistája.
A mesterséges agonista szerkezetileg annyira hasonlít a receptor természetes agonistájához, hogy ugyanolyan hatással lehet a receptorra. Sok gyógyszert természetes agonisták utánzására készítenek, hogy azok a receptorokhoz kötődjenek, és ugyanazt - vagy sokkal erősebb - reakciót válthassanak ki.
Egyszerűen fogalmazva, az agonista olyan, mint a kulcs, amely illeszkedik a zárba (a receptor), és elfordítja, hogy kinyissa az ajtót (vagy biokémiai vagy elektromos jelet küldjön a hatás kifejtéséhez). A természetes agonista a fő kulcs, de lehetséges más kulcsok (agonista gyógyszerek) tervezése, amelyek ugyanazt a feladatot végzik.
A morfiumot például nem a test tervezte, de természetesen megtalálható az ópiummákban. Szerencsére utánozza a természetes opioid agonisták, az endorfinok alakját, amelyek természetes fájdalomcsillapítók, amelyek felelősek az „endorfin magasért”.
Különleges hatások, például fájdalomcsillapítás vagy eufória fordulnak elő, mivel az opioid receptorok csak az agy és a test egyes részein vannak jelen, amelyek befolyásolják ezeket a funkciókat.
A kannabisz fő hatóanyaga, a THC a kannabinoid receptor agonistája, a hallucinogén LSD pedig egy szintetikus molekula, amely utánozza a szerotonin neurotranszmitter agonista hatását számos receptorának egyikén - az 5HT2A receptoron.
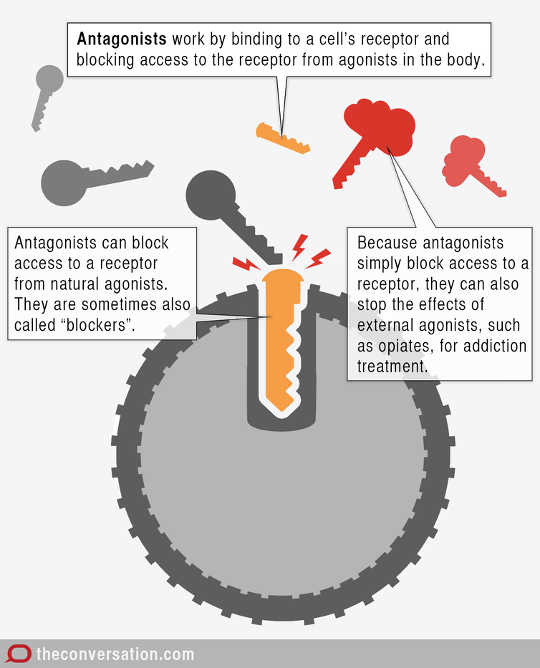
 CC BY-ND antagonista gyógyszerekAz antagonista olyan gyógyszer, amely közvetlenül ellenzi az agonista hatását.
CC BY-ND antagonista gyógyszerekAz antagonista olyan gyógyszer, amely közvetlenül ellenzi az agonista hatását.
Ismét a zár és a kulcs analógiáját használva az antagonista olyan, mint egy kulcs, amely szépen illeszkedik a zárba, de nincs megfelelő alakja a zár elfordításához. Ha ezt a kulcsot (antagonistát) behelyezzük a zárba, a megfelelő kulcs (agonista) nem mehet be ugyanabba a zárba.
Tehát az agonista hatását blokkolja az antagonista jelenléte a receptor molekulában.
Ismét gondoljunk a morfinra, mint az opioid receptor agonistájára. Ha valaki potenciálisan halálos morfintúladagolást tapasztal, az opioid receptor antagonista naloxon megfordíthatja a hatásokat.
Ennek oka az, hogy a naloxon (Narcan néven forgalmazva) gyorsan elfoglalja a test összes opioidreceptorát, és megakadályozza a morfin kötődését és aktiválását.
A morfium másodpercek alatt pattog be és ki a receptoron. Ha nem kötődik a receptorhoz, az antagonista bejuthat és blokkolhatja azt. Mivel a receptor nem aktiválható, ha egy antagonista elfoglalja a receptort, nincs reakció.
A Narcan hatása drámai lehet. Még akkor is, ha a túladagolás áldozata eszméletlen vagy a halál közelében van, az injekció beadása után másodperceken belül teljesen tudatos és éber lehet.
 Membrán transzport inhibitorok
Membrán transzport inhibitorok
A membrán transzporterek nagy fehérjék, amelyek a sejt membránjába vannak ágyazva, és kisebb molekulákat - például neurotranszmittereket - szállítanak a sejt kívülről, amely felszabadítja őket, és visszafelé. Egyes gyógyszerek gátolják hatását.
A szelektív szerotonin -visszavétel -gátlók (SSRI -k) - például az antidepresszáns fluoxetin (Prozac) - így működnek.
A szerotonin egy agyi neurotranszmitter, amely szabályozza a hangulatot, az alvást és egyéb funkciókat, például a testhőmérsékletet. Az idegvégződésekből szabadul fel, és az agy közeli sejtjeinek szerotonin -receptorához kötődik.
A folyamat zökkenőmentes működése érdekében az agynak gyorsan ki kell kapcsolnia a szerotoninból érkező jeleket, miután a vegyszerek felszabadultak a terminálokról. Ellenkező esetben lehetetlen lenne az agy és a test működésének pillanatról pillanatra történő ellenőrzése.
Az agy ezt az idegterminális membránban lévő szerotonin transzporterek segítségével teszi. A szállítók, mint a porszívó, felveszik a szerotonin molekulákat, amelyek nem kötődnek a receptorokhoz, és visszaszállítják őket a terminál belsejébe későbbi használatra.
Az SSRI gyógyszerek úgy működnek, hogy beszorulnak a vákuumtömlőbe, így a nem kötött szerotonin molekulák nem szállíthatók vissza a terminálba.
Mivel ezután több szerotonin molekula lóg tovább a receptorok körül, továbbra is stimulálják őket.
Nyersen elmondhatjuk, hogy az extra szerotonin mérsékelten növeli a jel hangerejét, hogy fokozza a pozitív hangulatot. De a tényleges módja a depresszióra és a szorongásra sokkal bonyolultabb.
Az összes gyógyszernek körülbelül 40% -a csak egy receptorcsaládot céloz meg - a G-fehérje kapcsolt receptorok. Ezeknek a gyógyszermechanizmusoknak vannak eltérései, beleértve a részleges agonistákat és azokat, amelyek antagonistaként hatnak, de kissé eltérően. Összességében azonban sok kábítószer -kezelés a fent leírt kategóriákba tartozik.
A szerzőről
 MacDonald Christie, a Sydney -i Egyetem farmakológiai professzora. egy celluláris és molekuláris neurofarmakológus, amelynek kutatási területei közé tartozik az opioid receptor jelátviteli sejtes és molekuláris mechanizmusai neuronokban és szinapszisok a fájdalom útvonalaiban, a krónikus fájdalmat és kábítószer -függőséget okozó adaptációk biológiai alapja, valamint a conotoxinokból származó új fájdalomterápiák preklinikai fejlesztése.
MacDonald Christie, a Sydney -i Egyetem farmakológiai professzora. egy celluláris és molekuláris neurofarmakológus, amelynek kutatási területei közé tartozik az opioid receptor jelátviteli sejtes és molekuláris mechanizmusai neuronokban és szinapszisok a fájdalom útvonalaiban, a krónikus fájdalmat és kábítószer -függőséget okozó adaptációk biológiai alapja, valamint a conotoxinokból származó új fájdalomterápiák preklinikai fejlesztése.
Ezt a cikket eredetileg közzétették A beszélgetés. Olvassa el a eredeti cikk.
Kapcsolódó könyvek
at InnerSelf Market és Amazon























